Proprietăți elastice
La fel ca în majoritatea celorlalte proprietăți ale metalelor cu pământuri rare, modulele elastice ale metalelor cu pământuri rare se încadrează în procentul mijlociu al celorlalte elemente metalice. Valorile pentru scandiu și litiu sunt aproximativ aceleași cu cele ale membrilor finali ai lantanidelor (erbiu până la lutetiu). Există o creștere generală a modulului elastic odată cu creșterea numărului atomic. Sunt evidente valorile anomale pentru ceriu (unele legături 4f) și ytterbiu (divalență).
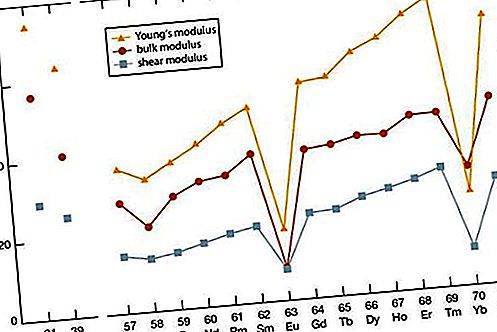
Proprietăți mecanice
Metalele cu pământuri rare nu sunt nici elemente metalice slabe, nici mai ales puternice și prezintă o ductilitate modestă. Deoarece proprietățile mecanice depind destul de puternic de puritatea metalelor și de istoricul lor termic, este dificil să se compare valorile raportate în literatură. Puterea finală variază de la aproximativ 120 până la aproximativ 160 MPa (megapascali) și ductilitate de la aproximativ 15 la 35%. Rezistența ytterbium (europium nu a fost măsurată) este mult mai mică, 58 MPa, iar ductilitatea este mai mare, aproximativ 45%, așa cum s-ar fi așteptat pentru metalul divalent.
Proprietăți chimice
Reactivitatea metalelor cu pământuri rare cu aerul prezintă o diferență semnificativă între lantanidele ușoare și cele grele. Lantanidele ușoare se oxidează mult mai rapid decât lantanidele grele (gadoliniu prin lutetiu), scandiu și ittriu. Această diferență se datorează în parte variației produsului de oxid format. Lantanidele ușoare (lantanul prin neodim) formează structura hexagonală R 2 O 3 de tip A; lantanidele mijlocii (samariu prin gadoliniu) formează faza R monoclinică de tip R 2 O 3; în timp ce lantanidelor grele, scandiu și ytriu formă cubic tip C R 2 O 3 modificare. Tipul A reacționează cu vaporii de apă din aer pentru a forma un oxidroxid, ceea ce determină acoperirea albă să se scurgă și permite oxidarea să continue prin expunerea suprafeței metalului proaspăt. Oxidul de tip C formează o acoperire strânsă și coerentă care împiedică oxidarea suplimentară, similar cu comportamentul aluminiului. Samariul și gadoliniu, care formează faza R 2 O 3 de tip B, se oxidează puțin mai repede decât cele mai grele lantanide, scandiu și irtriu, dar formează în continuare un înveliș coerent care oprește oxidarea ulterioară. Din această cauză, lantanidele ușoare trebuie păstrate în vid sau într-o atmosferă cu gaz inert, în timp ce lantanidele grele, scandiul și ytriumul pot fi lăsate afară în aer liber, ani de zile, fără oxidare.
Europium metal, care are o structură de ccc, oxidează cel mai rapid oricare dintre pământurile rare cu aer umed și trebuie manipulat în orice moment într-o atmosferă cu gaz inert. Produsul de reacție al europiu când este expus la aer umed este un hidrat hidroxid de sodiu, Eu (OH) 2 -H 2 O, care este un produs de reacție neobișnuită, deoarece toate celelalte metale de pământuri rare formează un oxid.
Metalele reacționează puternic cu toți acizii cu excepția acidului fluorhidric (HF), eliberând H 2 gaz și formarea compusului de pământuri rare-anion corespunzător. Metalele cu pământuri rare, atunci când sunt plasate în acid fluorhidric, formează o acoperire RF 3 insolubilă care împiedică orice reacție suplimentară.
Metalele de pământuri rare reacționează ușor cu hidrogen gazos, pentru a forma RH 2 și, în condiții puternic hydriding, RH 3 faza cu excepția scandiu, care nu formează un trihydride.
compuşi
Elementele de pământuri rare formează zeci de mii de compuși, cu toate elementele din dreapta și inclusiv a grupurilor de metale 7 (mangan, tecetiu și reniu) din tabelul periodic, plus beriliu și magneziu, care se află la distanță partea stângă în grupul 2. Seriile importante de compuși și unii compuși individuali cu proprietăți unice sau comportamente neobișnuite sunt descriși mai jos.
Oxizii
Cea mai mare familie de compuși anorganici de pământuri rare studiați până în prezent sunt oxizii. Cea mai stoechiometria comună este R 2 O 3 compoziție, dar, deoarece câteva elemente lantanide au alte stări de valență, în plus față de 3+, există pentru alte stoichiometrii exemplu, oxid de ceriu (CeO 2), oxid de praseodim (Pr 6 O 11), oxid de terbiu (Tb 4 O 7), oxid de europiu (EuO) și Eu 3 O 4. Cea mai mare parte a discuțiilor se va concentra pe oxizii binari, dar vor fi examinați pe scurt oxizii ternari și alți de ordin superior.