Borane, oricare dintr-o serie omologă de compuși anorganici de bor și hidrogen sau derivații acestora.
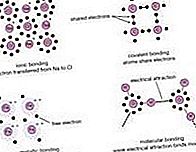
lipire chimică: Borane
Dibranul compus cu deficiență de electroni, B2H6, așa cum s-a menționat anterior, poate fi privit ca un grup de atomi întreținuți
Hidridii de bor au fost sintetizați și caracterizați în primul rând sistematic în perioada 1912 până la aproximativ 1937 de chimistul german Alfred Stock. El le-a numit borane în analogie cu alcani (hidrocarburi saturate), hidrurile de carbon (C), care este vecinul borului din tabelul periodic. Deoarece boranele mai ușoare erau volatile, sensibile la aer și umiditate și toxice, Stock a dezvoltat metode și aparate cu vid ridicat pentru studierea lor. Lucrările americane la borane au început în 1931, efectuate de Hermann I. Schlesinger și Anton B. Burg. Boranes a rămas în primul rând de interes academic până în cel de-al Doilea Război Mondial, când guvernul SUA a sprijinit cercetările pentru a găsi compuși volanți de uraniu (borohidride) pentru separarea izotopilor și anii '50, când a susținut programe pentru dezvoltarea de combustibili cu energie mare pentru rachete și avioane cu jet. (Borane și derivații lor au o căldură de combustie mult mai mare decât combustibilii cu hidrocarburi.) William Nunn Lipscomb, Jr., a primit Premiul Nobel pentru Chimie din 1976 „pentru studiile sale asupra structurii boranelor care luminează probleme de legătură chimică”, în timp ce unul dintre Schlesinger studenții, Herbert Charles Brown, au împărtășit premiul 1979 pentru reacția sa de hidroborare (1956), adăugarea remarcabil de ușoară a BH3 (sub forma de BH 3 · S) la compuși organici nesaturați (adică alchene și alchine) în solvenți eter (S) la temperatura camerei pentru a produce organoborane cantitativ (adică într-o reacție care se desfășoară în totalitate sau aproape în întregime, până la finalizare). La rândul său, reacția de hidroborare a deschis noi căi de cercetare în domeniul sintezei organice stereospecifice.
Boranele care au fost preparate de Stock au avut compoziția generală B n H n + 4 și B n H n + 6, dar se cunosc specii mai complexe, atât neutre, cât și negative (anionice). Hidrurile de bor sunt mai numeroase decât cele ale oricărui alt element, cu excepția carbonului. Cea mai simplă borană izolabilă este B 2 H 6, diborană (6). (Numărul arabesc din paranteze indică numărul de atomi de hidrogen.) Este unul dintre cei mai studiați și cei mai utili intermediari chimici. Este disponibil comercial și de ani de zile multe borane și derivații lor au fost preparate din acesta, direct sau indirect. Free BH 3 (și B 3 H 7) sunt foarte instabile, dar ele pot fi izolate ca aducți stabile (produse de adiție) cu baze Lewis (molecule electron donor) -ex, BH 3 · N (CH 3) 3. Boranele pot fi solide, lichide sau gaze; în general, punctele lor de topire și fierbere cresc odată cu creșterea complexității și a greutății moleculare.
Structura și lipirea boranelor
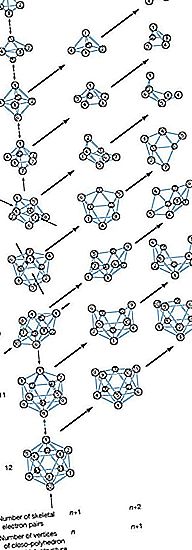
În loc să prezinte configurațiile simple de lanț și inel ale compușilor de carbon, atomii de bor din boranele mai complexe sunt localizați la colțurile poliedrelor, care pot fi considerați fie ca deltaedre (poliedre cu fețe triunghiulare), fie fragmente deltaedrice. Dezvoltarea unei înțelegeri a acestor grupuri de bor a făcut mult pentru a-i ajuta pe chimiști să raționalizeze chimia altor compuși anorganici, organometalici și de tranziție a metalelor de tranziție.
Unul din mai multe sisteme de nomenclatură sugerate de Uniunea Internațională de Chimie Pură și Aplicată (IUPAC) folosește prefixuri structurale caracteristice: (1) closo- (o corupție a „clovo”, din latină clovis, însemnând „cușcă”), deltaedre de n atomi de bor; (2) nido- (din nidus latină, însemnând „cuib“), structuri nonclosed în care B n clusterul ocupă n colțuri ale unui (n + 1) -cornered poliedru-adică un closo-poliedru cu un singur nod lipsă; (3) arachno- (greacă, însemnând „pânză de păianjen”), grupuri care sunt și mai deschise, cu atomi de bor care ocupă n colțuri contigue ale unui poliedru (n + 2) cu culoarea - adică, un închidere-poliedru cu două vârfuri lipsă.; (4) hipo- (greacă, însemnând „a țese” sau „o rețea”), cele mai deschise ciorchini, cu atomi de bor care ocupă n colțurile unui (n + 3) closo-poliedru acoperit; și (5) klado- (greacă, însemnând „ramură”), n vârfuri ale unui n + 4-vertex closo-poliedru ocupat de n atomi de bor. Membrii seriei hipo- și klado- sunt cunoscuți în prezent doar ca derivați boranici. Legătura dintre două sau mai multe dintre aceste clustere borane poliedrice este indicată prin prefixul conjunctiv- (latin, care înseamnă „unire”). De exemplu, conjuncto-B 10 H 16 este produs prin aderarea la B 3 H 8 unități de două B 6 H 9 molecule printr - o legătură B-B.
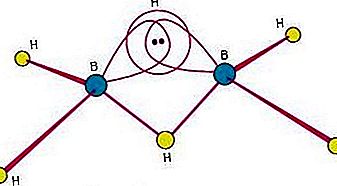
Unul dintre motivele marelui interes pentru borane este faptul că posedă structuri diferite de oricare altă clasă de compuși. Deoarece legarea în borane implică legarea multicentrică, în care trei sau mai mulți atomi împart o pereche de electroni de legătură, boranele sunt numite în mod obișnuit substanțe cu deficiență de electroni. Diborane (6) are următoarea structură:
Această structură implică o legătură cu trei centri, în care o pereche de electroni este împărțită între trei (mai degrabă decât doi) atomi - doi atomi de bor și un atom de hidrogen. (Vezi legătura chimică: Aspecte avansate ale legării chimice: Borane pentru o discuție a legăturii cu trei centri.) Capacitatea borului de a forma astfel de legături în plus față de legăturile covalente normale duce la formarea boranelor poliedrice complexe.