Aminoacizi standard
Una dintre cele mai utile maniere prin care se poate clasifica aminoacizii standard (sau comuni) se bazează pe polaritatea (adică pe distribuția sarcinii electrice) a grupului R (de exemplu, lanțul lateral).
Grupa I: aminoacizi nepolari
Aminoacizii din grupa I sunt glicina, alanina, valina, leucina, izoleucina, prolina, fenilalanina, metionina și triptofanul. Grupele R ale acestor aminoacizi au fie grupări alifatice, fie aromatice. Acest lucru le face hidrofobe („frică de apă”). În soluții apoase, proteinele globulare se vor plia într-o formă tridimensională pentru a îngropa aceste lanțuri laterale hidrofobe în interiorul proteinei. Structurile chimice ale aminoacizilor din grupa I sunt:
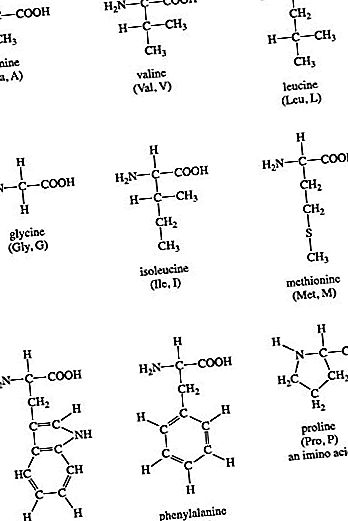
Isoleucina este un izomer al leucinei și conține doi atomi de carbon chiral. Prolina este unică printre aminoacizii standard, prin faptul că nu are atât grupe a-amino libere, cât și a-carboxilice libere. În schimb, lanțul său lateral formează o structură ciclică, deoarece atomul de azot al prolinei este legat de doi atomi de carbon. (Strict vorbind, aceasta înseamnă că prolina nu este un aminoacid, ci mai degrabă un acid α-imino.) Fenilalanina, după cum sugerează și numele, constă dintr-o grupare fenil atașată la alanină. Metionina este unul dintre cei doi aminoacizi care posedă un atom de sulf. Metionina joacă un rol central în biosinteza proteinelor (traducere) deoarece este aproape întotdeauna aminoacidul inițiator. Metionina oferă, de asemenea, grupuri metil pentru metabolism. Tryptofan conține un inel indol atașat la lanțul lateral alanyil.
Grupa II: aminoacizi polari, neîncărcați
Aminoacizii din grupa II sunt serina, cisteina, treonina, tirozina, asparagina și glutamina. Lanțurile laterale din acest grup posedă un spectru de grupuri funcționale. Cu toate acestea, cei mai mulți au cel puțin un atom (azot, oxigen sau sulf) cu perechi de electroni disponibili pentru legarea hidrogenului la apă și alte molecule. Structurile chimice ale aminoacizilor din grupa II sunt:

Doi aminoacizi, serină și treonină, conțin grupări hidroxil alifatice (adică un atom de oxigen legat la un atom de hidrogen, reprezentat ca „OH). Tirosina are o grupare hidroxil în inelul aromatic, ceea ce îl face un derivat al fenolului. Grupările hidroxil din acești trei aminoacizi sunt supuse unui tip important de modificare post-translațională: fosforilare (vezi mai jos aminoacizi non-standard). Ca și metionina, cisteina conține un atom de sulf. Spre deosebire de atomul de sulf de metionină, cu toate acestea, sulful cisteinei este foarte reactiv chimic (vezi mai jos oxidarea cisteinei). Asparagina, izolată mai întâi de sparanghel și glutamină ambele conțin grupe amide R. Gruparea carbonil Funcția poate ca acceptor de legături de hidrogen, iar gruparea amino (NH 2) poate funcționa ca un donor de legături de hidrogen.
Grupa III: Acizi aminoacizi
Cei doi aminoacizi din această grupă sunt acidul aspartic și acidul glutamic. Fiecare are un acid carboxilic pe lanțul său lateral care îi conferă proprietăți acide (donatoare de protoni). Într-o soluție apoasă la pH fiziologic, toate cele trei grupări funcționale pe acești aminoacizi se vor ioniza, oferind astfel o încărcare totală de -1. În formele ionice, aminoacizii sunt numiți aspartat și glutamat. Structurile chimice ale aminoacizilor din grupa III sunt

Lanțurile laterale ale aspartatului și glutamatului pot forma legături ionice („punți de sare”) și pot funcționa, de asemenea, ca acceptoare de legături cu hidrogen. Multe proteine care leagă ionii de metal („metaloproteine”) în scopuri structurale sau funcționale posedă situri de legare a metalelor care conțin lanțuri laterale de aspartat sau glutamat sau ambele. Glutamatul liber și glutamina joacă un rol central în metabolismul aminoacizilor. Glutamatul este cel mai abundent neurotransmițător excitator din sistemul nervos central.