Adăugarea nucleofilelor de carbon
O mare varietate de nucleofili de carbon se adaugă la aldehide și astfel de reacții au o importanță primordială în chimia organică sintetică, deoarece produsul este o combinație de două scheleturi de carbon. Chimiștii organici au reușit să adune aproape orice schelet de carbon, oricât de complicat, prin utilizarea ingenioasă a acestor reacții. Unul dintre cele mai vechi și mai importante este adăugarea reactivilor Grignard (RMgX, unde X este un atom de halogen). Chimistul francez Victor Grignard a câștigat Premiul Nobel pentru chimie din 1912 pentru descoperirea acestor reactivi și reacțiile lor.
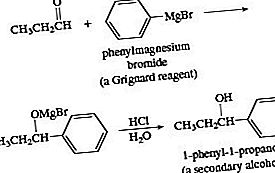
Adăugarea unui reactiv Grignard la o aldehidă urmată de acidifierea în acidul apos dă un alcool. Adăugarea la formaldehidă dă un alcool primar. Adăugarea la o aldehidă în afară de formaldehidă dă un alcool secundar.
Un alt nucleofil de carbon este ionul de cianură, CN -, care reacționează cu aldehide pentru a da, după acidificare, cianohidrine, compuși care conțin o grupare OH și CN pe același atom de carbon.
Cianhidrina de benzaldehidă (mandelonitril) oferă un exemplu interesant de mecanism de apărare chimică în lumea biologică. Această substanță este sintetizată de milipede (Apheloria corrugata) și depozitată în glandele speciale. Când un milipede este amenințat, cianhidrina este secretată de glanda sa de stocare și suferă disocierea catalizată de enzimă pentru a produce hidrogen cianură (HCN). Millipede eliberează apoi gazul HCN în mediul său înconjurător pentru a îndepărta prădătorii. Cantitatea de HCN emisă de un singur milipede este suficientă pentru a ucide un șoarece mic. Mandelonitrilul se găsește și în migdale amare și gropi de piersici. Funcția sa nu este cunoscută.
Alte reacții importante din această categorie includ reacția Knoevenagel, în care nucleofilul de carbon este un ester cu cel puțin un a-hidrogen. În prezența unei baze puternice, esterul pierde un α-hidrogen pentru a da un carbon încărcat negativ, care apoi se adaugă carbonului carbonil al unei aldehide. Acidificarea urmată de pierderea unei molecule de apă dă un ester α, β nesaturat.
O altă reacție de adăugare care implică un nucleofil de carbon este reacția Wittig, în care o aldehidă reacționează cu o fosforană (numită și ilură de fosfor), pentru a da un compus care conține o legătură dublă carbon-carbon. Rezultatul unei reacții Wittig este înlocuirea oxigenului carbonil al unei aldehide cu gruparea de carbon legată de fosfor. Chimistul german Georg Wittig a împărțit Premiul Nobel pentru chimie din 1979 pentru descoperirea acestei reacții și dezvoltarea utilizării sale în chimia organică sintetică.
Compușii conținând o grupă trimetilsilil (-SiMe 3, unde Me este gruparea metil, -CH 3) și un litiu (Li) atom pe același atom de carbon reacționează cu aldehide în așa-numita reacția Peterson pentru a da aceleași produse care ar se obține printr-o reacție Wittig corespunzătoare.
Deplasare la α-carbon
α-Halogenarea
Un α-hidrogen al unei aldehide poate fi înlocuit cu un atom de clor (CI), brom (Br) sau iod (I) atom când compusul este tratat cu CI 2, Br 2, sau I 2, respectiv, fie fără catalizator sau în prezența unui catalizator acid.
Reacția poate fi oprită ușor după ce se adaugă doar un atom de halogen. α-Halogenarea are loc de fapt sub forma enolului (vezi mai sus Proprietățile aldehidelor: Tautomerism) ale aldehidei și nu asupra aldehidei în sine. Aceeași reacție are loc dacă se adaugă o bază, dar nu poate fi oprită până când toți halogenii α atașați la același carbon nu au fost înlocuiți cu atomi de halogen. Dacă există trei alfa-hidrogeni același carbon, reacția merge un pas mai departe, având ca rezultat scindarea unui X 3 C - ion (unde X este un halogen) și formarea sării unui acid carboxilic.

Această reacție se numește reacție haloformă, deoarece ioni X 3 C - reacționează cu apa sau cu un alt acid prezent în sistem pentru a produce compuși de forma X 3 CH, care sunt numiți haloformi (de exemplu, CHCl 3 se numește cloroform).