Franciu (Fr), cel mai greu element chimic din grupa 1 (Ia) din tabelul periodic, grupa metalelor alcaline. Există doar în forme radioactive de scurtă durată. Franciul natural nu poate fi izolat în cantități vizibile, care pot fi cântărite, deoarece doar 24,5 grame (0,86 uncie) apar în orice moment pe întreaga crustă a Pământului. Existența franciului a fost prezisă de chimistul rus Dmitri I. Mendeleiev în clasificarea sa periodică a elementelor. Chimistul francez Marguerite Perey a descoperit franciul (1939) în timp ce a studiat actinium-227, care se degradează prin degradare beta negativă (emisie de electroni) la un izotop de toriu (toriu-227) și prin emisie alfa (aproximativ 1 la sută) într-un izotop de franciu (francium-223) care a fost numită anterior actinium K (AcK) și este un membru al seriei de decădere actinium. Deși este izotopul cel mai longeviv al franciului, franciul-223 are un timp de înjumătățire de numai 22 de minute. Treizeci și patru de izotopi de franciu cu mase cuprinse între 199 și 232 au fost pregătiți în mod artificial și, din moment ce franciul natural nu poate fi concentrat, este, de asemenea, preparat prin iradierea neutronică a radiului pentru a produce actinium, care se degradează să producă urme de franciu. Chimia franciului poate fi studiată numai prin metode proiectate pentru cantități. În toate privințele, comportamentul observat, inclusiv starea de oxidare de +1, este acela de așteptat ca un element alcalin să umple un loc chiar sub cesiu în tabelul periodic al elementelor. Aproape că nu există informații despre aspectele sale biologice.
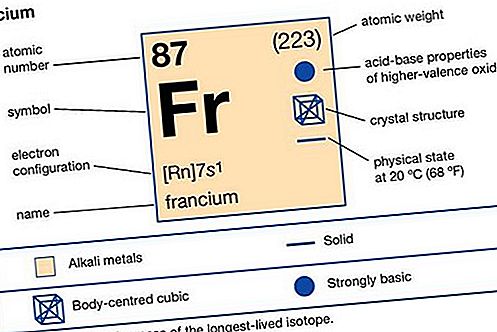

metal alcalin
cesiu (Cs) și franciu (Fr). Metalele alcaline sunt așa numite, deoarece reacția cu apa formează alcalii (adică baze puternice capabile
.Proprietățile elementului
| numar atomic | 87 |
|---|---|
| izotopul cel mai stabil | (223) |
| stare de oxidare | +1 |
| configurarea electronilor. | 2-8-18-32-18-8-1 sau [Rn] 7s 1 |